Lombalgie et douleur dans la jambe : le nerf est-il coupable ?

La lombalgie qui irradie dans la jambe n'est pas toujours liée à une douleur neuropathique. Il peut s'agir d'une douleur nociceptive. L'ABSG Mathera vous propose de lire une étude qui aide à différencier ces 2 mécanismes de douleur.
 |
AuteursAntoine Fourré, Félix Monnier, Laurence Ris, Frédéric Telliez, Jef Michielsen, Nathalie Roussel & Renaud Hage |
Définition de la douleur nociceptive et neuropathique
Les patients souffrant de lombalgie (LBP) ressentent souvent une douleur qui irradie dans la jambe. Environ deux tiers des patients qui consultent pour une lombalgie dans le cadre des soins primaires et secondaires présentent une douleur associée à la jambe [1,2]. Les professionnels de santé (PS) utilisent souvent des termes tels que « sciatique », « radiculopathie », « douleur radiculaire », « douleur pseudo-radiculaire », « douleur référée » et « pseudo-sciatalgie » pour désigner ces symptômes [3-8]. Cependant, un tableau clinique similaire peut avoir des mécanismes de douleur sous-jacents différents et qui se superposent (voir figure 1) [9]. Cette diversité de terminologie et cette superposition des mécanismes de la douleur sont non seulement source de confusion pour les patients et les professionnels de la santé, mais ils rendent également le processus de raisonnement clinique plus difficile et plus compliqué. Les objectifs de cet article sont donc (1) de clarifier et de décrire les mécanismes sous-jacents de la douleur tels que définis par l'Association internationale pour l'étude de la douleur (IASP) [1] et (2) d'aider les cliniciens à différencier le mécanisme de douleur prédominant en utilisant des scénarios cliniques.

Fig. 1 : Description de deux body-charts. Patient 1 & Patient 2 : ces patients décrivent la même topographie de douleur, localisée dans le bas du dos et qui irradie dans la jambe. L’intensité de la douleur est de 5/10 pour chaque patient sur l’échelle numérique de la douleur (NPRS).
Bien que l'expérience de la douleur soit extrêmement courante, il n'existe pas de consensus scientifique pour définir cette expérience. Cela n'est pas surprenant, étant donné la complexité de la douleur et les multiplicité des facteurs influençants. Cependant, cet article utilise la terminologie de l'IASP pour décrire les mécanismes de douleur sous-jacents. Cette organisation propose des définitions distinctes pour différencier la douleur nociceptive et la douleur neuropathique [10]. Ces deux types de mécanismes de douleur peuvent expliquer les douleurs de jambe liées à la lombalgie.
La douleur nociceptive
La douleur nociceptive est définie par l'IASP comme "une douleur qui résulte d'une atteinte ou d'une atteinte potentielle d'un tissu non nerveux et qui est due à l'activation des nocicepteurs. Les nocicepteurs sont activés par des stimuli mécaniques, chimiques ou thermiques provenant de toutes les structures innervées" [11,12].
La stimulation nociceptive des structures innervées de la colonne lombaire (par exemple les articulations zygapophysaires, les ligaments ou les muscles spinaux, ou la partie externe du disque lombaire) peut induire la transduction d'un stimulus nociceptif en un signal électrique dans le système nerveux. Ce signal, souvent appelé signal d'alarme, sera traité dans le système nerveux central avec des excitations cérébrales importantes [13] et peut conduire à la douleur [5,14,15]. Dans le cas de la douleur nociceptive, le système nerveux somato-sensoriel fonctionne normalement [16].
Chez certains patients, la douleur est également ressentie dans la jambe, à partir d'une région topographiquement différente de la source de la nociception [7]. Ce phénomène est considéré comme une douleur référée et pourrait être expliqué par la convergence des afférences nociceptives sur des neurones de second ordre. Le plus souvent, la douleur est perçue dans des régions qui ont la même innervation segmentaire. En outre, la douleur référée nociceptive peut également, dans certains cas, s'étendre jusqu'au pied [5].
La douleur neuropathique
L'IASP définit la douleur neuropathique comme "une douleur causée par une lésion ou une maladie du système nerveux somatosensoriel" [12,17].
La douleur neuropathique est un syndrome causé par diverses maladies ou lésions. La cause la plus fréquente de la douleur neuropathique chez les patients souffrant de lombalgie est liée à la compression des structures nerveuses (par exemple, une hernie discale) qui entraîne une inflammation ou une dégénérescence des fibres nerveuses [18-20]. Le système nerveux est affecté par la génération de décharges ectopiques qui court-circuitent la transduction [9]. Ces perturbations peuvent affecter la fonction nerveuse et entraîner des déficits sensoriels et moteurs.
Ces patients signalent souvent que la douleur dans la jambe est lancinante et irradie vers le bas dans une distribution radiculaire spécifique [21]. La douleur dans la jambe est généralement pire que la douleur dans le dos [21].
Comment différencier la douleur référée nociceptive et la douleur neuropathique ?
Il est crucial pour les cliniciens de déterminer quel est le mécanisme de douleur prédominant dans la fesse et/ou la jambe. Ne pas différencier les mécanismes responsable de la douleur irradiante dans l'évaluation des patients souffrant de lombalgie conduit à des investigations et des traitements inappropriés [18,22]. La douleur dans la jambe n'implique pas toujours une lésion ou une maladie des racines nerveuses ou du système nerveux périphérique [23-25]. La prise en charge des douleurs prédominantes nociceptives ou neuropathiques diffère d'un patient à l'autre [26]. La partie suivante détaillera donc comment distinguer ces mécanismes de la douleur.
Différencier la douleur neuropathique prédominante de la douleur référée nociceptive est un défi clinique. Bien que le diagnostic soit actuellement peu standardisé, les douleurs neuropathiques sont généralement identifiées sur la base de critères cliniques [27,28]. Le test quantitatif sensoriel (QST) pourrait être un outil utile, mais le QST est principalement utilisé dans les études de recherche [27]. Il consiste en plusieurs tests destinés à quantifier la fonction somatosensorielle (gain ou perte) chez les individus, mais il n'est pas suffisant à lui seul pour le diagnostic de la douleur neuropathique [29,30]. Le QST n'est pas largement utilisé par les praticiens de première ligne, tels que les kinésithérapeutes, pour plusieurs raisons : il prend du temps, il est extrêmement coûteux et il y a un manque de normes d'utilisation et d'interprétation [30]. Le diagnostic de douleur neuropathique dans les soins de première ligne est difficile à établir mais certains éléments de l'histoire du patient peuvent suggérer la présence ou l'absence de douleur neuropathique. Aucun d'entre eux n'est pathognomonique, mais le regroupement des éléments de l'anamnèse à partir de l'examen subjectif et objectif est le meilleur moyen de réduire le risque d'un diagnostic erroné [31]. Les cliniciens devraient principalement fonder leur stratégie diagnostique sur l'identification du mécanisme de douleur prédominant. La prochaine partie de cette revue narrative couvrira l'aspect théorique d'un examen subjectif (SE) et objectif (OE), accompagné d'une évaluation clinique à partir des patients présentés dans la figure 1.
Examen subjectif (ES)
Les symptômes décrits par le patient constituent la première étape de la théorisation du mécanisme de douleur prédominant. L'écoute des patients est importante dans le processus de différenciation, car les mots utilisés par les patients pour décrire leur douleur seront variables entre les patients souffrant de douleurs neuropathiques et nociceptives [27]. La figure 2 énumère les descriptions cliniques les plus courantes des douleurs neuropathiques et nociceptives exprimées par les patients.
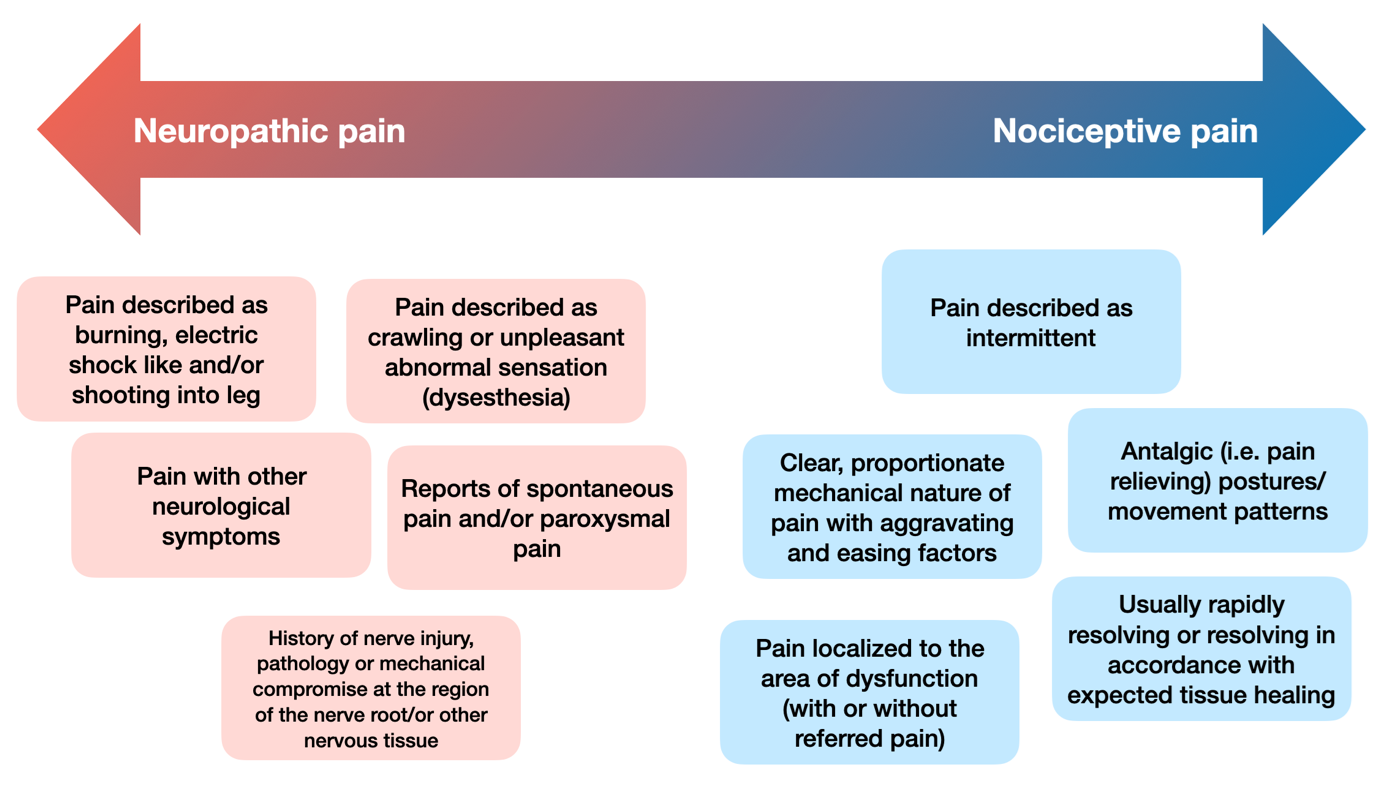
Fig. 2 : Consensus des descriptions cliniques pour la douleur neuropathique et nociceptive basée sur Mistry et al., 2020 [40] et Smart et al., 2011 [48].
Les douleurs neuropathiques sont généralement décrites dans une distribution liée à un dermatome ou cutanée [32]. Les descripteurs de la douleur les plus courants utilisés par les patients sont les brûlures, la douleur lancinante, et la douleur accompagnée de fourmillements inhabituels, d'une sensation de lourdeur, d'une décharge électrique ou la jambe qui tire [9,26,27]. La description d'un patient souffrant de douleurs neuropathiques est souvent caractérisée par des symptômes neurologiques spécifiques, tels que des signes sensoriels positifs (hyperalgésie et/ou allodynie) et négatifs (perte de fonction) [16,33]. Le patient peut éprouver diverses sensations, comme une paresthésie, une hypersensibilité mécanique ou thermique. La douleur neuropathique se caractérise également par des douleurs spontanées (survenant sans stimulation), évoquées (réponses anormales à des stimuli) ou paroxystiques (récurrences et intensifications soudaines) [32,34].
Ces symptômes contrastent avec la description des patients souffrant de douleurs nociceptives (référées). La douleur est généralement localisée dans la zone de la lésion ou de la dysfonction (avec ou sans douleur référée) [32]. Les symptômes sont généralement décrits comme intermittents et aigus lors des mouvements. La douleur est proportionnelle et en relation directe avec les facteurs de soulagement/aggravation [32]. Pour affiner le raisonnement dans l'ES, un certain nombre de questionnaires à remplir par le patient avec ou sans examen clinique (par exemple DN4, LANSS, PDQ) [34-37] ont été développés pour détecter la présence de douleurs neuropathiques, chacun ayant des caractéristiques spécifiques [38]. Le questionnaire « Douleur Neuropathique en 4 questions » (DN4) (sensibilité 0,83 ; spécificité 0,9) a été développé pour différencier la douleur neuropathique de la douleur nociceptive et semble avoir des caractéristiques psychométriques spécifiques pour la lombalgie [35]. Le questionnaire est court et ne contient que 10 items, qui s'il donne un score supérieur ou égal à 4, indique la présence probable d'une douleur neuropathique. Sept items sont utilisés comme questionnaire d'auto-évaluation des descripteurs sensoriels et 3 items sont notés sur la base de l'examen objectif (OE). La rapidité et la facilité d'utilisation d'un questionnaire tel que le DN4 en font un outil complémentaire précieux pour les cliniciens. Cependant, les questionnaires ne doivent pas remplacer un examen subjectif et objectif détaillé. Bien que de nombreux outils de dépistage aient une bonne sensibilité et spécificité, ils ne parviendraient pas à diagnostiquer 10 à 20 % des patients souffrant de douleurs neuropathiques [38].
Interprétation du scénario clinique
En interrogeant le patient 1 sur la qualité de ses symptômes, le patient mentionne une douleur dans la fesse qui irradie dans la jambe associée à des sensations indolores, telles que des brûlures, des picotements et des fourmillements dans le mollet. Le patient précise en outre que ces sensations ont tendance à augmenter lorsque la douleur augmente dans la fesse. Concernant les facteurs aggravants ou atténuants, le patient explique que la douleur est aggravée lorsqu'il sort de la voiture lorsqu’il fléchit la nuque. Le patient remarque également que la douleur est facilement provoquée et met plus de temps à diminuer. La douleur est décrite comme « imprévisible » et peut réapparaître spontanément. La présence de signes neurologiques positifs, la description des symptômes et le fait que le patient 1 décrit la douleur comme imprévisible soutiennent l'hypothèse d'une douleur neuropathique prédominante [39].
En interrogeant le patient 2 sur la qualité des symptômes, le patient mentionne une douleur principalement localisée dans la fesse mais irradiant dans la jambe jusqu'au mollet. La douleur est décrite comme vive et sourde. Concernant les facteurs aggravants ou atténuants, la douleur s'aggrave dans toutes les positions assises avec une flexion lombaire. La douleur augmente lors du passage de la position assise à la position debout ou l’inverse. Le patient 2 a remarqué que, généralement, l'intensité de la douleur diminuait rapidement et surtout si la flexion lombaire était évitée (par exemple, en se reposant sur le canapé en position allongée). La présence de symptômes clairs et proportionnés, associés à des facteurs aggravants et atténuants, et le fait que le patient 2 ne décrive aucun symptôme neurologique positif ou négatif confirment l'hypothèse d'un mécanisme nociceptif prédominant [32].
Bien que les évaluations subjectives des patients 1 et 2 fournissent des informations utiles pour aider à définir le mécanisme de douleur prédominant sous-jacent, il est évident que cela n'est pas suffisant pour tirer une conclusion définitive concernant le mécanisme de la douleur. Les éléments de l'OE, tels que les tests neurologiques et neurodynamiques, sont nécessaires pour affiner l'hypothèse établie pendant l'OE et conduire le clinicien à un diagnostic différentiel.
Examen objectif (OE)
Un examen objectif complet comprend l'observation, l'examen des mouvements actifs et l'examen des mouvements physiologiques passifs et accessoires. Si un mécanisme de douleur neuropathique est suspecté, les cliniciens doivent mener l'OE avec prudence et inclure une évaluation neurologique des fonctions sensorielles, motrices et autonomes du patient afin d'identifier un dysfonctionnement neurologique potentiel (y compris l'hypoesthésie et le test de frottement du DN4) [7]. Dans ce cas, l'examen neurologique pourrait mettre en évidence une distribution neuroanatomique de la douleur, des signes et symptômes positifs et/ou négatifs (altération des réflexes, de la sensation et de la puissance musculaire) [40]. La présence d'une hyperalgésie/allodynie et/ou d'autres anomalies sensorielles pourrait indiquer la présence d'une douleur neuropathique. De plus, un examen neurodynamique doit être intégré à l'OE pour évaluer la mécano-sensibilité du système nerveux [41,42]. Un examen neurodynamique est positif lorsqu'il reproduit au moins les symptômes du patient et une modification de ces symptômes avec une différenciation structurelle positive [43-45]. Le test le plus courant pour les membres inférieurs est le test passif d'élévation de la jambe droite (SLR) [42]. Le SLUMP test est un autre test neurodynamique avec une sensibilité élevée (0,9) pour identifier les douleurs neuropathiques dans le membre inférieur [44]. Il faut noter que, bien que la plupart des tests neurodynamiques aient une bonne sensibilité, ils ont généralement une faible spécificité et ne devraient pas être utilisés isolément [46]. Cependant, il est possible d'augmenter la précision du diagnostic en combinant plusieurs tests neurodynamiques [46,47]. Des recherches supplémentaires sont nécessaires pour déterminer la combinaison la plus pertinente de tests neurodynamiques pour détecter la douleur neuropathique dans la lombalgie.
S'il n'y a pas de preuve lors des examens neurologiques et neurodynamiques pour suggérer la présence d'une douleur neuropathique et en présence de symptômes cohérents et proportionnels, alors le mécanisme prédominant est probablement une douleur nociceptive (référée) [48].
Interprétation du scénario clinique
Puisque l'ES du patient 1 suggère un mécanisme de douleur neuropathique prédominant, l'OE doit inclure un examen neurologique et neurodynamique complet. Lors de l'examen neurologique, le patient décrit une perte de sensation au toucher léger dans le mollet et le pied droits, ainsi qu'une hyperalgésie à la piqûre d'épingle par rapport à la jambe gauche. En ce qui concerne l'évaluation neurodynamique, étant donné la douleur ressentie lors de la flexion de la nuque, le test SLUMP est bien adapté pour évaluer la mécanosensibilité. Le test est positif chez le patient 1 avec une reproduction des symptômes et une différenciation structurelle positive. Les informations provenant de la SE et de l'OE du patient 1 suggèrent la présence d'un mécanisme de douleur neuropathique prédominant.
Les éléments recueillis dans le ES du patient 2 suggèrent la présence d'un mécanisme prédominant de douleur nociceptive. En donnant les éléments du ES, un OE comprenant des mouvements actifs et des mouvements passifs physiologiques et accessoires doit être réalisé. Pendant les mouvements actifs, la douleur du patient 2 augmente lorsqu'il se penche en avant et l'amplitude du mouvement est limitée. La douleur diminue rapidement lors du retour à la position de départ. Ce schéma est similaire lors des mouvements physiologiques. La douleur est reproduite à un endroit précis (L4-L5) avec une mobilisation unilatérale postéro-antérieure et diminue rapidement après. Les informations provenant de la ES et de l'OE du patient 2 suggèrent la présence d'un mécanisme prédominant de douleur nociceptive. Même si une douleur neuropathique prédominante n'est pas suspectée, un examen neurologique doit être effectué lorsqu'un patient présente une douleur afin de confirmer une fonction normale du système nerveux. Les cliniciens doivent rester attentifs à toute modification de la symptomatologie et effectuer des examens complémentaires si des composantes neuropathiques apparaissent lors du rendez-vous de suivi du patient. L'OE dans la pratique clinique n'est pas décrite de manière extensive dans cet article car l'objectif principal est d'aider les cliniciens à différencier les deux descripteurs prédominants de la douleur. La prise en charge du patient doit s'appuyer sur un cadre biopsychosocial (BPS) dynamique et centré sur le patient, incluant les différents aspects du modèle de la Classification internationale du fonctionnement (CIF) [49,50].
Mécanisme prédominant de la douleur
Les éléments du ES et de l'OE des patients 1 et 2 suggèrent, respectivement, la présence d'un mécanisme prédominant de douleur neuropathique et de douleur nociceptive référée (voir figure 3). Les exemples cliniques présentés sont plutôt clairs et faciles à différencier. Cependant, dans la pratique clinique, la différenciation entre les deux n'est pas si facile et le raisonnement clinique est parfois très complexe pour les patients souffrant de douleurs aux jambes liées à la lombalgie. Les descripteurs, comme les signes et symptômes cliniques peuvent prêter à confusion et se superposer. Bien que la distinction soit essentielle pour une prise en charge efficace, les douleurs neuropathiques et nociceptives ont plusieurs caractéristiques en commun. Les douleurs exclusivement nociceptives et neuropathiques peuvent en fait être très rares en pratique [3,51,52]. Toutes deux partagent les mêmes neurotransmetteurs, les mêmes voies spinales ascendantes, les mêmes régions supraspinales de traitement de l’information et les mêmes voies modulatrices descendantes [9]. Le point de vue classique selon lequel ces deux mécanismes sont des entités totalement distinctes est remise en question par certains experts et pourrait être due à notre propension à classer les éléments [9]. Dans la plupart des cas, il s'agit probablement d'une combinaison des deux mécanismes avec, selon les cas, une prédominance neuropathique ou nociceptive. Les cliniciens doivent être conscients que cette prédominance peut changer avec le temps (voir figure 2) et évaluer le patient de manière répétée au cours de séances consécutives.
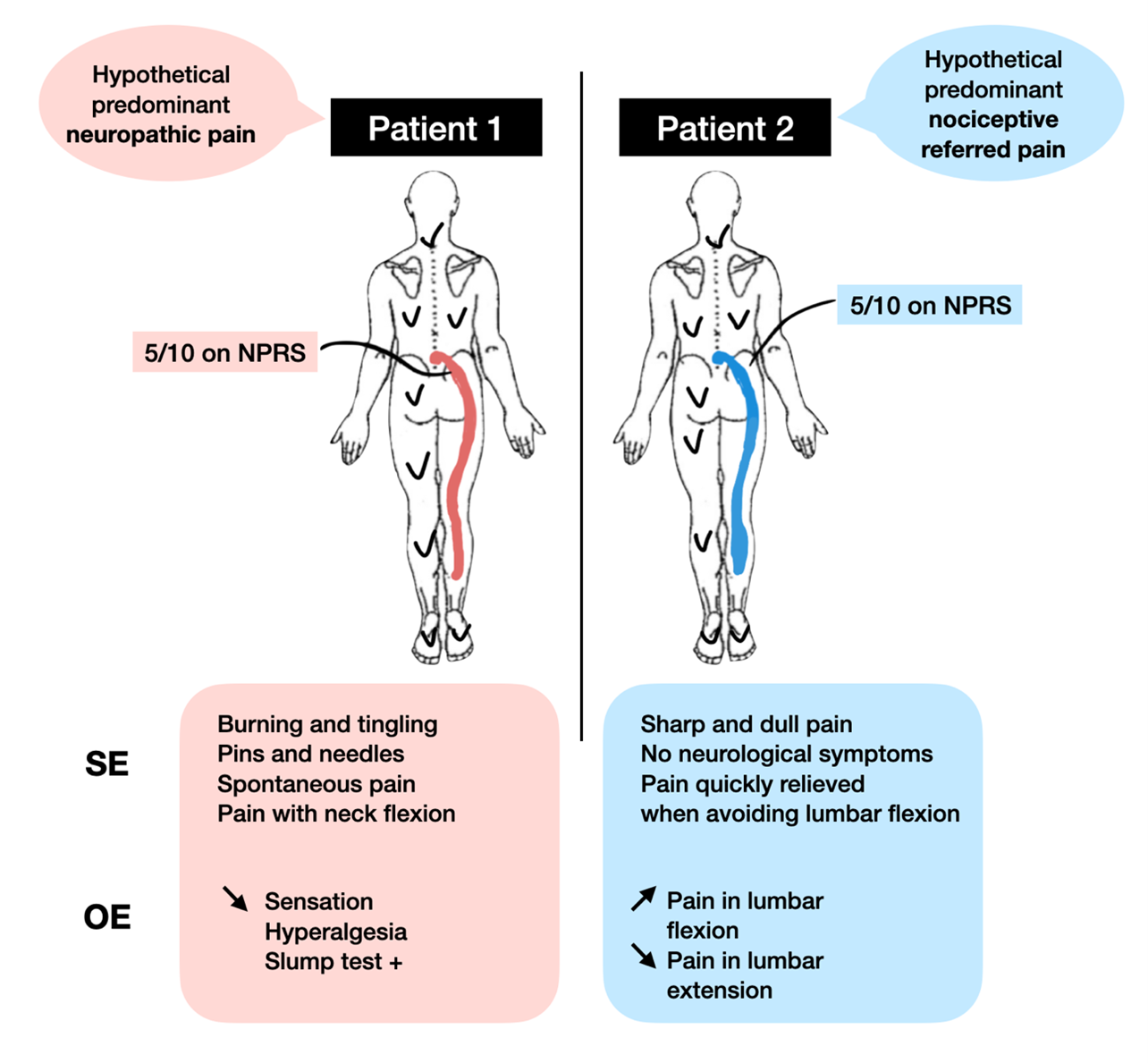
Fig. 3 : Body chart du patient 1 et patient 2 après un examen subjectif et physique complet
Discussion et conclusion
L'objectif de cet article est de discuter de la prédominance des mécanismes douloureux sous-jacents aux douleurs de jambe liées à la lombalgie et d'aider les cliniciens à différencier ces mécanismes dans la pratique clinique. La distinction entre douleur neuropathique et nociceptive est essentielle pour établir une prise en charge adaptée et centrée sur le patient. Si le clinicien se contente d'évaluer la topographie de la douleur (par exemple, irradiation dans la fesse), ces deux mécanismes de douleur sont facilement confondus et peuvent conduire à des investigations et une prise en charge inappropriées [5,22]. Bien que la topographie des symptômes puisse être similaire, la description et le comportement de la douleur complétés par un examen objectif approfondi doivent être utilisés pour différencier les mécanismes de douleur prédominants. Cependant, la terminologie utilisée dans la littérature semble difficile à transposer de la recherche à la pratique clinique. De plus, la pratique clinique est complexe, et parfois cette différenciation semble trop simpliste et insuffisante. Ces mécanismes douloureux ne doivent pas être considérés comme des entités distinctes [9]. Des superpositions existent entre ces deux descripteurs de la douleur et pourraient expliquer les difficultés à mettre en place un traitement basé sur le mécanisme [9]. Certains patients présentent des composantes nociceptives prédominantes mais peuvent simultanément présenter des symptômes suggérant une composante neuropathique. L'état d'un patient n'est pas figé dans le temps et doit être évalué à plusieurs reprises au cours du suivi par une combinaison d'examens subjectifs et objectifs afin de déterminer le mécanisme de douleur prédominant. Ceci est cliniquement important car le pronostic d'un patient souffrant de douleur neuropathique est moins bon que celui d'un patient souffrant de douleur nociceptive et doit conduire le clinicien à une prise en charge adaptée [2]. Ainsi, la prise en charge d'un patient présentant une douleur neuropathique prédominante comprend des médicaments spécifiques [53], des traitements passifs adaptés [41,43,54], un dosage approprié des exercices [55] et une éducation sur le fonctionnement du système nerveux [43]. De plus, le clinicien doit être conscient des changements potentiels dans la symptomatologie du patient afin de prévenir l'aggravation potentiellement grave du problème de santé [56]. D'autres recherches sont nécessaires pour mieux définir le diagnostic, le pronostic et les parcours des patients souffrant de douleurs aux jambes liées à la lombalgie.
Sources :
Low-back related leg pain: is the nerve guilty? How to differentiate the underlying pain mechanism. : J Man Manip Ther, 1-7. doi:10.1080/10669817.2022.2092266
Fourre, A., Monnier, F., Ris, L., Telliez, F., Michielsen, J., Roussel, N., & Hage, R. (2022)
Article publié en Open Access dans « Journal of Manual & Manipulative Therapy » (Fourre et al., 2022)
Références
[1] Hill JC, Konstantinou K, Egbewale BE, et al. Clinical outcomes among low back pain consulters with referred leg pain in primary care. Spine (Phila Pa 1976). 2011 Dec;36(25):2168–2175.
[2] Harrisson SA, Stynes S, Dunn KM, et al. Neuropathic pain in low back-related leg pain patients: what is the evidence of prevalence, characteristics, and prognosis in primary care? A systematic review of the literature. J Pain. 2017 Nov;18(11):1295–1312.
[3] Freynhagen R, Rolke R, Baron R, et al. Pseudoradicular and radicular low-back pain – a disease continuum rather than different entities? Answers from quantita- tive sensory testing. Pain. Mar;135(1):65–74.
[4] Van Boxem K, Van Zundert J, Patijn J, et al. Pseudoradicular and radicular low-back pain: how to diagnose clinically? Pain. Apr;135(3):311–312.
[5] Bogduk N. On the definitions and physiology of back pain, referred pain, and radicular pain. Pain. Dec;147(1):17–19.
[6] Valat J-P, Genevay S, Marty M, et al. Sciatica. Best Pract Res Clin Rheumatol. Apr;24(2):241–252.
[7] Baron R, Binder A, Attal N, et al. Neuropathic low back pain in clinical practice. Eur J Pain. 2016 Jul;20 (6):861–873.
[8] Beynon R, Elwenspoek MMC, Sheppard A, et al. The utility of diagnostic selective nerve root blocks in the management of patients with lumbar radiculopathy: a systematic review. BMJ Open. 2019 Apr;9(4):e025790.
[9] Cohen SP, Mao J. Neuropathic pain: mechanisms and their clinical implications. BMJ. Feb 5;348(feb05 6):f7656–f7656.
[10] Scholz J, Finnerup NB, Attal N, et al. The IASP classifica- tion of chronic pain for ICD-11: chronic neuropathic pain. PAIN. Jan;160(1):53–59.
[11] Merskey H, Bogduk N. Part III: pain Terms: a current list with definitions and notes on usage. In: Classif chronic pain. Second ed. 2011; p. 209–214.
[12] Terminology | international association for the study of pain [Internet]. cited 2022 Mar 3]. Available from:
[13] Marchand S. The physiology of pain mechanisms: from the periphery to the Brain. Rheumatol Dis Clin N Am. May;34(2):285–309.
[14] Tsao H, Tucker KJ, Coppieters MW, et al. Experimentally induced low back pain from hypertonic saline injections into lumbar interspinous ligament and erector spinae muscle. Pain. Jul;150(1):167–172.
[15] O’Neill S, Graven-Nielsen T, Manniche C, et al. Ultrasound guided, painful electrical stimulation of lumbar facet joint structures: an experimental model of acute low back pain. Pain. Jul;144(1):76–83.
[16] La Cesa S, Tamburin S, Tugnoli V, et al. How to diag- nose neuropathic pain? The contribution from clinical examination, pain questionnaires and diagnostic tests. Neurol Sci. Dec;36(12):2169–2175.
[17] Jensen TS, Baron R, Haanpää M, et al. A new definition of neuropathic pain. Pain. Oct;152(10):2204– 2205.
[18] Schäfer A, Hall T, Briffa K. Classification of low back- related leg pain—A proposed patho-mechanism- based approach. Man Ther. Apr;14(2):222–230.
[19] Yoshizawa H, Kobayashi S, Morita T. Chronic nerve root compression: pathophysiologic mechanism of nerve root dysfunction. Spine (Phila Pa 1976). 1995 Feb;20 (supplement):397–407.
[20] Freynhagen R, Baron R, Tölle T, et al. Screening of neuropathic pain components in patients with chronic back pain associated with nerve root compression: a prospective observational pilot study (MIPORT). Curr Med Res Opin. 2006 Mar;22(3):529–537.
[21] Koes BW, van Tulder MW, Peul WC. Diagnosis and treat- ment of sciatica. BMJ. 2007 Jun 23;334(7607):1313–1317. [22] Schäfer A, Hall T, Müller G, et al. Outcomes differ between subgroups of patients with low back and leg pain following neural manual therapy: a prospective cohort study. Eur Spine J. 2011 Mar;20(3):482–490.
[23] Konstantinou K, Dunn KM, Ogollah R, et al. Characteristics of patients with low back and leg pain seeking treatment in primary care: baseline results from the ATLAS cohort study. BMC Musculoskelet Disord. 2015 Dec;16(1):332.
[24] Saifuddin A, Emanuel R, White J, et al. An analysis of radiating pain at lumbar discography. Eur Spine J. 1998 Oct 19;7(5):358–362.
[25] O’Neill CW, Kurgansky ME, Derby R, et al. Disc stimula- tion and patterns of referred pain. Spine (Phila Pa 1976). 2002 Dec;27(24):2776–2781.
[26] Haanpää ML, Backonja -M-M, Bennett MI, et al. Assessment of neuropathic pain in primary care. Am J Med. 2009 Oct;122(10):S13–S21.
[27] Bouhassira D. Neuropathic pain: definition, assessment and epidemiology. Rev Neurol (Paris). 2019 Jan;175(1– 2):16–25.
[28] Smith BH, Torrance N, Bennett MI, et al. Health and quality of life associated with chronic pain of predo- minantly neuropathic origin in the community. Clin J Pain. 2007 Feb;23(2):143–149.
[29] Rolke R, Magerl W, Campbell KA, et al. Quantitative sensory testing: a comprehensive protocol for clinical trials. Eur J Pain. 2006 Jan;10(1):77.
[30] Birklein F, Sommer C. Quantitative sensory testing—a tool for daily practice? Nat Rev Neurol. 2013 Sep;9 (9):490–492.
[31] Callin S, Bennett MI. Assessment of neuropathic pain. Contin Educ Anaesth Crit Care Pain. 2008 Dec;8 (6):210–213.
[32] Smart KM, Blake C, Staines A, et al. Mechanisms-based classifications of musculoskeletal pain: part 2 of 3: symptoms and signs of peripheral neuropathic pain in patients with low back (±leg) pain. Man Ther. 2012 Aug;17(4):345–351.
[33] Zilliox LA. Neuropathic Pain. Contin Lifelong Learn Neurol [Internet]. 2017;23(2). Available from: https:// journals.lww.com/continuum/Fulltext/2017/04000/ Neuropathic_Pain.13.aspx
[34] Bennett M. The LANSS pain scale: the Leeds assess- ment of neuropathic symptoms and signs. Pain. 2001 May;92(1):147–157.
[35] Bouhassira D, Attal N, Alchaar H, et al. Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain. 2005 Mar;114 (1):29–36.
[36] Nikaido T, Sumitani M, Sekiguchi M, et al. The Spine painDETECT questionnaire: development and valida- tion of a screening tool for neuropathic pain caused by spinal disorders. Ikeda K, editor. PLOS ONE. 2018 Mar 21;13(3):e0193987.
[37] Haanpää M, Attal N, Backonja M, et al. NeuPSIG guide- lines on neuropathic pain assessment. Pain. 2011 Jan;152(1):14–27.
[38] Cruccu G, Sommer C, Anand P, et al. EFNS guidelines on neuropathic pain assessment: revised 2009: neuro- pathic pain assessment. Eur J Neurol. 2010 Aug;17 (8):1010–1018.
[39] Koury MJ, Scarpelli E. A manual therapy approach to evaluation and treatment of a patient with a chronic lumbar nerve root irritation. Phys Ther. 1994 Jun 1;74 (6):548–560.
[40] Mistry J, Falla D, Noblet T, et al. Clinical indicators to identify neuropathic pain in low back related leg pain: a modified Delphi study. BMC Musculoskelet Disord. 2020 Dec;21(1):601.
[41] Shacklock M. Neurodynamics. Physiother Elsevier. 1995 Jan 1;81(1):9–16.
[42] Boyd BS, Wanek L, Gray AT, et al. Mechanosensitivity of the lower extremity nervous system during straight-leg raise neurodynamic testing in healthy individuals. J Orthop Sports Phys Ther. 2009 Nov;39(11):780–790.
[43] Nee RJ, Butler D. Management of peripheral neuro- pathic pain: integrating neurobiology, neurodynamics, and clinical evidence. Phys Ther Sport. Feb;7 (1):36–49.
[44] Urban LM, MacNeil BJ. Diagnostic accuracy of the slump test for identifying neuropathic pain in the lower limb. J Orthop Sports Phys Ther. Aug;45 (8):596–603.
[45] Nee RJ, Jull GA, Vicenzino B, et al. The validity of upper-limb neurodynamic tests for detecting periph- eral neuropathic pain. J Orthop Sports Phys Ther. 2012 May;42(5):413–424.
[46] van der Windt DA, Simons E, Riphagen II, et al. Physical examination for lumbar radiculopathy due to disc her- niation in patients with low-back pain. Cochrane back and neck group, editor. Cochrane Database Syst Rev [Internet]. 2010 Feb 17; [cited 2021 Nov 2]. 10.1002/ 14651858.CD007431.pub2
[47] González Espinosa de Los Monteros FJ, Gonzalez- Medina G, Ardila EMG, et al. Use of neurodynamic or orthopedic tension tests for the diagnosis of lumbar and lumbosacral radiculopathies: study of the diag- nostic validity. Int J Environ Res Public Health. Oct;17(19):7046. PMID:32993094.
[48] Smart KM, Blake C, Staines A, et al. The discriminative validity of “Nociceptive,” “Peripheral Neuropathic,” and “Central Sensitization” as mechanisms-based clas- sifications of musculoskeletal pain. Clin J Pain. Oct;27(8):655–663.
[49] Jull G. Biopsychosocial model of disease: 40 years on. Which way is the pendulum swinging? Br J Sports Med. Aug;51(16):1187–1188.
[50] World Health Organization. International classification of functioning, disability and health: ICF. Classif Int Fonct handicap santé CIF [Internet] Geneva: World Health Organization; . [cited 2021 Sep]. Available from:
[51] Toda K. Pure nociceptive pain is very rare. Curr Med Res Opin. Nov 2;35(11):1991.
[52] Freynhagen R. on behalf of the author group. Response: letter: pure nociceptive pain is very rare. Curr Med Res Opin. Dec 2;35(12):2137.
[53] Attal N. Pharmacological treatments of neuropathic pain: the latest recommendations. Rev Neurol (Paris). Jan;175(1–2):46–50.
[54] Jones MA, Rivett D. Clinical reasoning in musculoske- letal practice - E-Book [Internet]. Elsevier Health Sciences; . [cited 2021 Mar]. Available from:
[55] Leitzelar BN, Koltyn KF. Exercise and Neuropathic Pain: a General Overview of Preclinical and Clinical Research. Sports Med - Open. Dec;7(1):21.
[56] Finucane LM, Downie A, Mercer C, et al. International framework for red flags for potential serious spinal pathologies. J Orthop Sports Phys Ther. 2020 May 21;1–23. 10.2519/jospt.2020.9971.











.png)






